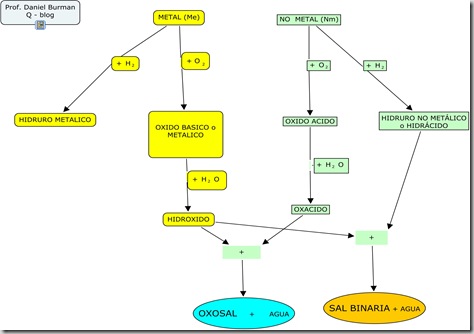
metal(+) + H(+1) o no + no metal (+) + O (-2) = oxisal
Para el nombre, ya no son los mismos sufijos, el oso cambia a ito, y el ico cambia a ato, esto es para el caso de el no metal, el metal si no cambia sus sufijos
Para el nombre primero se pone el nombre del no metal con sus respectivos sufijos y prefijos ya cambiados los sufijos, después ácido (si es que hay hidrógeno, sino no), y después el metal con sus sufijos y prefijos
Se toma un radical de un oxiácido, y se le agrega el metal
ácido carbónico-> H₂CO₃
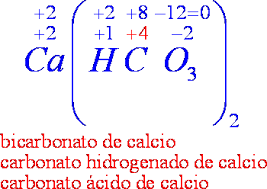
Pb(HCO₃)₂ -> carbonato ácido plumboso
se tomo el ácido carbónico, y se le quitó un hidrógeno, volviéndolo un radical negativo, y se le agragó un metal para hacerlo neutro
 ->
-> 
 ->
->